Activer le mode zen
Ressource au format PDF
Mots-clés
Classification
Nouvelles méthodes d'imagerie pour le cerveau
Les radiotraceurs pour l'imagerie nucléaire en neurologie
25/03/2024
Résumé
Cet article présente la tomographie par émission de positons, à l'aide d'isotopes radioactifs.
Table des matières
Retrouvez les autres articles du dossier « Nouvelles méthodes d'imagerie pour le cerveau » :
1. Les radiotraceurs pour l'imagerie nucléaire en neurologie
La tomographie par émission de positons (TEP) [1][2] repose sur la détection de la radioactivité émise par certains atomes appelés « isotopes radioactifs ». Ces isotopes radioactifs ont le même nombre de protons que les isotopes stables correspondants, mais un nombre de neutrons différent. Les plus utilisés aujourd'hui sont le carbone 11 et le fluor 18. Ainsi le carbone 11 est un isotope radioactif du carbone 12 stable qui compose l'essentiel de la matière vivante. Le carbone 11 et le fluor 18 n'existent pas naturellement, ils sont créés à l'intérieur d'accélérateurs de particules appelés cyclotrons. Au sein de ces cyclotrons, une réaction nucléaire, c'est-à-dire touchant le noyau des atomes, va générer ces atomes radioactifs en modifiant le noyau d'autres atomes. Ainsi, le fluor 18 est produit à partir d'oxygène 18 stable qui existe à l'état naturel. Après leur production, les isotopes radioactifs sont accrochés sur des molécules, comme par exemple du sucre (glucose) ou des médicaments grâce à des réactions chimiques (« radio-chimie »). L'ensemble isotope-radiotraceur constitue un radiotraceur qui est alors injecté dans le sang. Ces aspects sont détaillés dans la conférence de notre collègue Didier Le Bars [2].
Fonctionnement de la tomographie par émission de positon (TEP)
La radioactivité au service de la médecine : imagerie par tomographie à émission de positons, une conférence de Didier Le Bars Source : CultureSciences Physique [2]. |
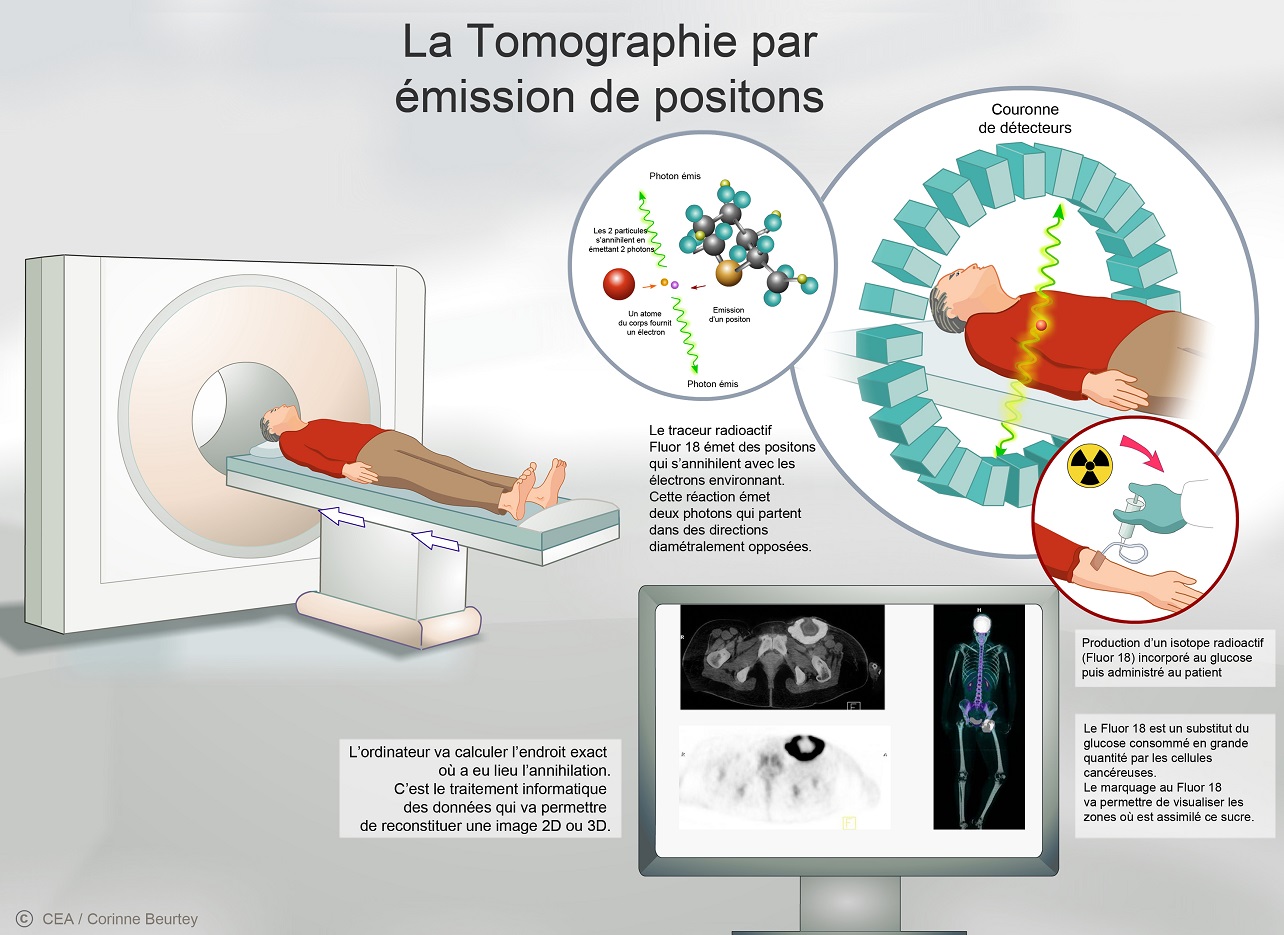
La tomographie par émission de positons (TEP) Source : Corinne Beurtey/CEA, Dossier sur l'imagerie médicale le site du CEA [1]. |
Lien vers une vidéo de présentation de la tomographie par émission de positons (TEP) Source : Corinne Beurtey/CEA, Tomographie par emission de positons [1]. |
Les isotopes radioactifs vont se désintégrer en émettant une particule appelée positon (électron positif). Lorsque ce positon rencontre dans la matière un électron (deux particules de même masse mais de charge opposée), les deux s'annihilent et disparaissent en créant de l'énergie selon la formule connue E = mc2. L'énergie créée E est égale à la masse m des deux particules, multipliée par la vitesse de la lumière c au carré.
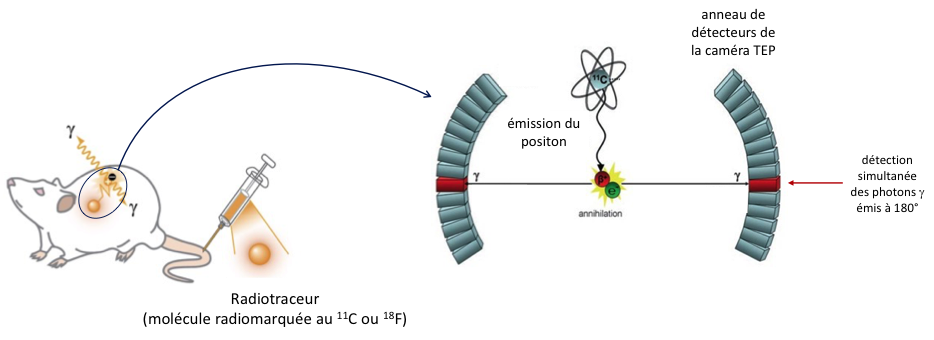
Cette énergie E prend la forme de deux rayons gamma émis à 180° l'un de l'autre. Ce sont ces rayons gamma qui sont captés par la caméra TEP, elle-même constituée d'une couronne de détecteurs sensibles à la radioactivité, figure 1. C'est la détection simultanée des deux rayons gamma qui permet à la caméra de reconstituer l'origine de la réaction d'annihilation et ainsi créer une image.
L'imagerie TEP occupe une place majeure en médecine pour le diagnostic des patients atteints de cancer, et en neurosciences pour l'étude du cerveau, organe difficilement accessible autrement que par l'imagerie, figure 2.
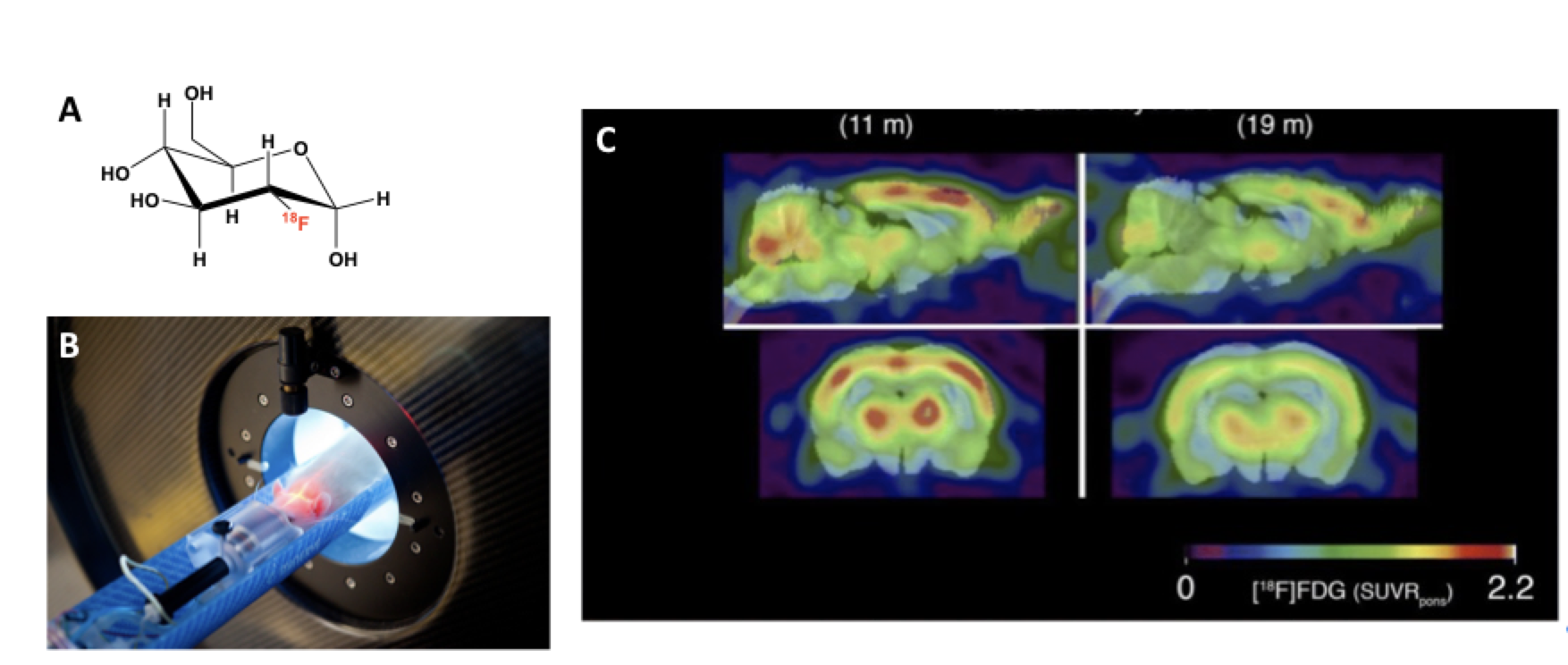
Le cerveau est un organe qui utilise énormément de glucose pour fonctionner. Ainsi, le glucose radiomarqué au fluor 18 ([18F]FDG), figure 2A, est un radiotraceur de l'activité du cerveau, on appelle cela le métabolisme cérébral. Le [18F]FDG est injecté au rat placé dans une caméra TEP dédiée aux petits animaux, figure 2B. On peut ainsi étudier les variations du métabolisme cérébral provoquées par des maladies comme la maladie d'Alzheimer. Un modèle de rat utilisé pour étudier cette maladie neurodégénérative a été imagé deux fois, à 11 mois et 19 mois, figure 2C. On remarque une nette diminution de la fixation du [18F]FDG dans le cerveau du rat, révélant une baisse du métabolisme cérébral provoqué par la progression de la maladie.
La video associée montre l'acquisition TEP 3D superposée à l'image du scanner X (montrant les os du crâne).
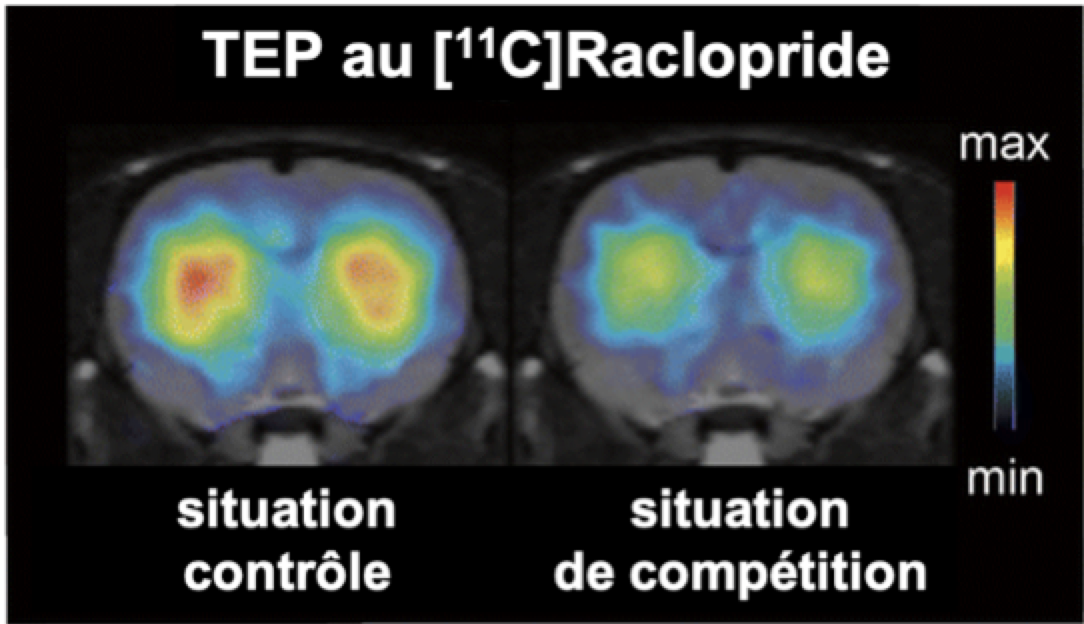
On utilise aussi l'imagerie TEP pour étudier la chimie du cerveau. Sur la figure 3, le radiotraceur [11C]Raclopride est utilisé pour visualiser les récepteurs d'un neurotransmetteur appelé Dopamine. Les récepteurs de la Dopamine sont les cibles des drogues appelées psychostimulants telles que la cocaïne ou les amphétamines. On peut le vérifier sur l'image de droite où une amphétamine a été injectée juste avant le radiotraceur. Les deux molécules, amphétamine et [11C]Raclopride sont en compétition au niveau des récepteurs de la dopamine provoquant ainsi la baisse de signal observée.
Figure 3. L'imagerie TEP permet d'étudier la neurochimie in vivo On observe ici une intoxication aux amphétamines qui provoque une baisse de fixation du radiotraceur. Source : Herfert K, Mannheim JG, Kuebler L, et al. [7]. |
On notera que l'imagerie TEP ne donne aucune information anatomique et de ce fait elle est souvent accompagnée d'une imagerie anatomique tel que le scanner à rayon X ou l'IRM. Ces caméras hybrides TEP/scanner ou plus rarement TEP/IRM sont disponibles dans les services hospitaliers de médecine nucléaires, et les mêmes radiotraceurs peuvent être utilisés chez l'homme et chez l'animal de laboratoire. En cela, l'imagerie TEP permet une recherche véritablement « translationnelle », du laboratoire au lit du patient.
Retrouvez les autres articles du dossier « Nouvelles méthodes d'imagerie pour le cerveau »
Références
[1] Dossier sur l'imagerie médicale, CEA, consulté en septembre 2023.
[2] La radioactivité au service de la médecine : imagerie par tomographie à émission de positons, une conférence de Didier Le Bars, mai 2012, CultureSciences Physique - ISSN 2554-876X.
[3] A molecular imaging primer: modalities, imaging agents, and applications, James ML, Gambhir SS, Physiol Rev. 2012;92(2):897-965.
[4] Synthesis of 11C, 18F, 15O, and 13N radiolabels for positron emission tomography, Miller PW, Long NJ, Vilar R, Gee AD, Angew Chem Int Ed Engl. 2008;47(47):8998-9033.
[5] GIGA - CRC In VIvo Imaging, Université de Liège, Belgique.
[6] Consequences of Metabolic Disruption in Alzheimer's Disease Pathology, Ryu JC, Zimmer ER, Rosa-Neto P, Yoon SO, Neurotherapeutics, 2019;16(3):600-610.
[7] Quantitative Rodent Brain Receptor Imaging, Herfert K, Mannheim JG, Kuebler L, et al., Mol Imaging Biol. 2020;22(2):223-244.
Pour citer cet article :
Nouvelles méthodes d'imagerie pour le cerveau - Les radiotraceurs pour l'imagerie nucléaire en neurologie, Fabien Chauveau, Guillaume Becker, mars 2024. CultureSciences Physique - ISSN 2554-876X, https://culturesciencesphysique.ens-lyon.fr/ressource/Imagerie-TEP.xml