Activer le mode zen
Ressource au format PDF
Classification
L'osmose ou comment extraire l'énergie dans l'eau salée
12/01/2015
Résumé
Cet article présente le phénomène d'osmose et ses applications pour la création d'énergie renouvelable, il est tiré de « Fluides en mouvement, du monde macroscopique au nano-monde... et vice-versa », une conférence de Lydéric Bocquet donnée le 28 octobre 2014 pour le « Congrès 2014 de l'Union des Professeurs de Physique et Chimie », organisé à Lyon.
Table des matières
1. L'osmose, qu'est-ce que c'est ?
1.1 Définition et historique
En cuisine, lorsque l'on veut faire dégorger un concombre, on le saupoudre de sel. De cette façon cela crée une solution très salée à l'extérieur qui engendre un mouvement de l'eau du côté le moins salé vers le côté plus salé. Le concombre se comporte comme une membrane semi-perméable qui permet de laisser sortir l'eau sans laisser entrer le sel dans sa chair : c'est le phénomène d'osmose.
On retrouve ce phénomène d'osmose dans le vivant comme, par exemple, dans les filtres au niveau des reins (aquaporing) où chaque jour 200 L de plasma sont filtrés. Il est aussi utilisé dans beaucoup d'applications comme notamment les salaisons, où le sel vient absorber la quantité d'eau disponible pour les bactéries qui vont finir par périr.
Le point clé est que l'eau se déplace vers les zones salées. Ainsi le phénomène d'osmose réalise la conversion d'énergie chimique (car on est en présence d'un gradient de potentiel chimique) en énergie mécanique par le biais d'un écoulement de fluide qui va de la zone la moins salée vers la plus salée.
Loi de van't Hoff
Ce phénomène a été décrit pour la première fois par van't Hoff qui a reçu le prix Nobel de chimie en 1901 pour ses travaux sur l'osmose. La loi qu'il a proposée n'est ni plus ni moins que la loi des gaz parfaits, c'est-à-dire qu'il décrit l'osmose simplement comme une pression. C'est une loi très simple qui s'écrit :
Δ Π = RT ΔCsel
où Π représente la pression osmotique, R la constante des gaz parfaits, T la température en K et Csel la concentration en sel.
En guise d'illustration, si on dispose de deux fluides qui présentent une différence de salinité de 1 mol.L-1, de part et d'autre d'une surface semi-perméable qui ne laisse pas passer le sel, la différence de pression obtenue sera de l'ordre de 50 bar. C'est gigantesque et équivalent à un barrage de 500 m de hauteur. En prenant maintenant l'eau d'un fleuve et l'eau de mer, la différence de salinité est de 0,6 mol.L-1, cela induit une différence de pression de 30 bar.
1.2 L'osmose sous l'angle de la physique statistique
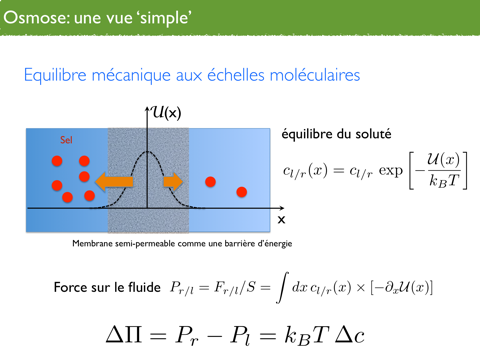
On peut apporter un autre éclairage sur la définition de l'osmose. Usuellement on la décrit en terme d'un équilibre de potentiels chimiques entre la phase saline et la phase sans sel, en disant que la solution s'équilibre des deux côtés. Ainsi lorsque la solution n'est pas au bon potentiel chimique du côté non salé, elle va transférer de l'eau pour diluer au maximum l'eau salé.
On peut voir cela peut-être plus simplement à l'aide de la physique statistique en montrant que toute la difficulté dans ce système et qui disparaît dans le résultat final, c'est le rôle de la membrane semi-perméable qui ne laisse passer que l'eau et pas le sel. Il suffit de voir cette membrane comme une barrière d'énergie pour le sel mais pas pour l'eau. Il est possible de décrire la distribution des particules de sel du soluté par une loi de Boltzmann. En présence d'une différence de profil de densité de salinité, on peut calculer la force exercée par la membrane sur le fluide. Cette force (en orange sur le schéma de la figure 2) s'exprime simplement comme le nombre de molécules de sel fois la force élémentaire par molécule. Quand on intègre cela de chaque côté de la membrane, on obtient effectivement une différence de pression.
C'est une description plus moléculaire mais qui permet d'aller plus loin. On peut, par exemple, réfléchir à des systèmes disymétriques ou des systèmes qui laissent peu passer le sel.
À partir de ce principe relativement élémentaire, on peut imaginer créer des diodes osmotiques, c'est-à-dire des diodes pour lesquelles l'eau passe dans le sens du gradient de salinité mais pas dans l'autre sens.
2. Générer de l'électricité
Maintenant comment allons-nous générer de l'électricité ?
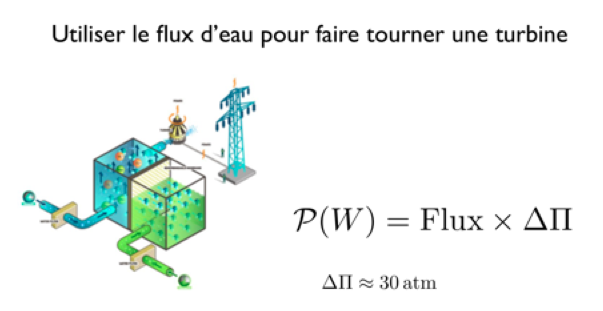
L'idée la plus simple et qui a été démontrée à une échelle pré-industrielle par une entreprise norvégienne, est d'utiliser de l'eau de mer d'un côté, de l'eau de rivière de l'autre côté, et de disposer une membrane semi-perméable entre les deux. Pour trouver l'équilibre l'eau de la rivière traverse la membrane vers le côté plus salé. Ainsi la colonne d'eau salée (en bleu sur la figure 3) monte et s'il y a un débordement, l'eau coule et fait tourner une turbine, générerant de l'électricité de cette façon.
Nouvelles pistes pour l'énergie renouvelable
Si on fait une estimation, au niveau mondial, de la quantité d'énergie contenue dans ces gradients de salinité, on est de l'ordre du Térawatt !
On donne pour comparaison que 1 Térawatt équivaut à l'énergie fournie par 1 000 réacteurs nucléaires ! C'est donc une piste à explorer.
Source : Nature, numéro 488 du 16 août 2012 « Membrane-based processes for sustainable power generation using water », Bruce E. Logan et Menachem Elimelec.
A consulter sur le thème des sources d'énergie :
- Mémento sur l'énergie 1, un mémento sur l'énergie pour faire le point sur les définitions et unités associées à l'énergie, dans le domaine de la physique, de la technologie, ainsi qu'en économie, compte tenu du débat actuel sur notre avenir énergétique.
- Mémento sur l'énergie 2, un article qui fournit des données quantitatives sur l'énergie solaire : son origine due à la fusion nucléaire de l'hydrogène, la quantité d'énergie produite, le spectre du rayonnement émis et la puissance reçue à la surface de la terre.
Deux grosses difficultés se présentent à l'heure actuelle pour le développement industriel de tels convertisseurs d'énergie renouvelable :
- la première consiste à trouver comment récupérer cette énergie de façon efficace, la géographie de la planète imposant souvent le ré-aménagement du territoire,
- l'autre grande difficulté réside dans la réalisation des membranes semi-perméables.
3. Des premiers tests grandeur nature
3.2 Les problèmes de rendement
Les premiers tests grandeurs nature ne donnent pas encore satisfaction. La grosse difficulté est posée par les membranes. La puissance est le flux d'eau fois la différence de pression, or ici la différence de pression est gigantesque mais pour que le sel ne traverse pas mais que l'eau traverse, il faut avoir une membrane qui a des pores nanométriques jusqu'à sub-nanométriques.
Avec des pores si petits, la perméabilité de la membrane est extrêmement faible ainsi le flux de l'eau traversant la membrane est très faible et la puissance que l'on peut récupérer de ce système se mesure en quelques W/m2 de membrane, ce qui n'est pas suffisant pour rendre le processus commercialement rentable (de l'ordre de 5 W/m2). Ce rendement a pu être atteind en utilisant des saumures issues de puits très profonds où la salinité de l'eau dépasse largement 1 à 2 mol.L-1. Par contre l'eau de mer qui est à 0,6 mol.L-1, n'est pas suffisante pour créer assez d'énergie avec ces membranes.
Donc comme la membrane est le point clé et qu'elle n'a, pour l'instant, pas été optimisée, on peut se demander si la connaissance du transport de fluide aux nanoéchelles ne peut pas proposer des solutions nouvelles.
3.2 Les opportunités données par les nouveaux matériaux
La bonne nouvelle est que de nouveaux matériaux font parler d'eux dans la littérature et semblent permettre de révolutionner ce domaine.
Dans un article paru dans la revue Science en 2006, les auteurs [Holt et al, 2006] ont fabriqué des membranes à base de nanotubes de carbone de 1 à 2 nanomètres de rayon. Ils ont mesuré la perméabilité de ces membranes, c'est-à-dire le flux pour une différence de pression donnée et ont trouvé qu'elle est jusqu'à 4 ordres de grandeur plus grande que ce que l'on attend par l'équation de Navier-Stokes.
On a pu montrer récemment que le nanotube de carbone est très particulier. Il possède une surface qui a une interaction assez neutre avec l'eau, mais les frottements entre les molécules d'eau et la matrice de carbone sont anormalement faibles. Cela vient du fait que la structure de l'eau est incommensurable par rapport à la structure du carbone. C'est comme si les deux structures ne s'appareillaient pas, ce qui réduit le frottement, exactement comme dans le cas d'un frottement solide-solide mais vu ici entre un fluide et un solide.
4. Réponse osmotique avec des nanotubes bore-azote
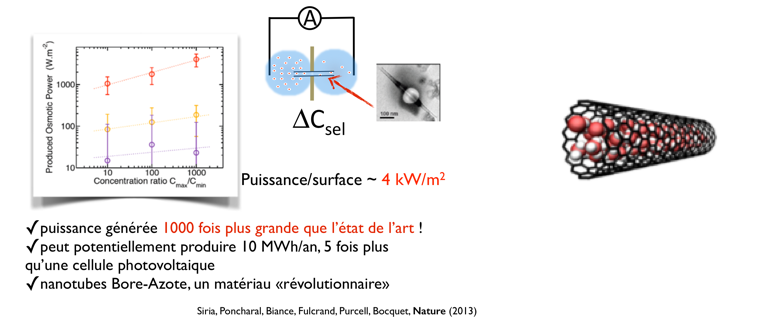
Nous avons effectué des recherches [Siria et al, 2013]à partir d'un seul nanotube, afin de bien comprendre les problématiques en jeu, pour ensuite développer des membranes de grandes tailles. Le nanotube est composé d'atomes de bore et d'azote, à la place de carbone pour des raisons techniques. Il mesure environ dix nanomètres de diamètre. Nous avons appliqué une différence de salinité de chaque côté du nanotube et nous avons mesuré le courant électrique généré. En analogie avec le potentiel chimique, le courant induit est proportionnel au gradient du logarithme de la concentration en sel. Il atteint ici une intensité de l'ordre du nanoampère.
On s'intéresse maintenant à la puissance produite avec cette technologie pour la comparer avec d'autres types de membranes. Le calcul de la puissance est obtenu en intégrant l'énergie sur toute la surface du nanotube. On trouve que l'on peut ici produire jusqu'à 4 kW/m2. Le chiffre qu'il faut retenir c'est que l'on atteint le kiloWatt contre quelques Watt, dans le cas des membranes de technologies différentes.
Ces très bons résultats sont aussi dûs à la spécificité très forte des matériaux bore et azote. De la même façon que les nanotubes de carbone montraient un caractère très particulier au niveau de la perméabilité, les nanotubes de bore-azote sont extrêmement singuliers du point de vue de leur interaction avec l'eau. Ces nanotubes présentent une charge de surface très grande, ce qui permet de convertir de façon très efficace la différence de salinité en courant électrique. Et cela ouvre énormément de perspectives pour le futur.
Il est intéressant de revenir à la question initiale, c'est-à-dire comment rendre efficace les processus osmotiques. Avec ce genre de membrane, on sait que l'on est capable d'y arriver. Les puissances obtenues ici sont complètement au-delà des puissances actuelles. Ces résultats ont été obtenus avec un seul nanotube, il reste à faire toute la démarche pour développer des membranes de nanotubes à grande échelle. Il faut maintenant intéresser des industriels.
Voir la conférence « Fluides en mouvement, du monde macroscopique au nano-monde... et vice-versa », par Lydéric Bocquet (2014), dont est tiré cet article.
Bibliographie
[Holt et al, 2006] « Fast mass transport through sub-2-nanometer carbon nanotubes », Holt et al, Science, numéro 312 du 19 mai 2006.
[Siria et al, 2013] « Giant osmotic energy conversion measured in a single transmembrane boron nitride nanotube », Siria et al, Science, numéro 494 du 28 février 2013.
Pour citer cet article :
L'osmose ou comment extraire l'énergie dans l'eau salée, janvier 2015. CultureSciences Physique - ISSN 2554-876X, https://culturesciencesphysique.ens-lyon.fr/ressource/osmose-Bocquet.xml